Pamatojoties uz saņemtu ziņojumu no Slovēnijas kompetentās iestādes, Veselības inspekcija (turpmāk-Inspekcija) informē patērētājus, izplatītājus un importētājus par prasībām neatbilstošiem, Slovēnijas tirgū konstatētiem vienreiz lietojamiem skābekļa piesātinājuma asinīs (SpO2) sensoriem, ražotājs Shenzhen Upnmed Equipment Co Ltd., kas neatbilst Eiropas Parlamenta un Padomes Regulas 2017/745, kas attiecas uz medicīniskām ierīcēm (turpmāk – Regula 2017/745) prasībām. Neatbilstošu sensoru REF kodi: U401-C, UD401-2AA, U401-2P, U401-2P, U401-2A, U401-2A, U421-3ES, U421-3ES, U421-3BS, U401-2DS, U401-2DS, U401-2ES, U401-2ES, U401-2ES, U401-2ES, U401-2ES, U401-2FS, U401-2HS, U401-2BS, U401-2BS, U401-2CS, U401-2CS, U401-2CS, U401-2CS, U472-3ES, U472-3ES, U472-3ES, U472-3ES, U472-3CS, U472-3CS, U472-3HS, U472-3HS, UD401-2I, UD401-2I, UD401-2N, UD401-2N, UD401-2N, UD401-2N.
Iesakām iepazīties ar neatbilstošo medicīniskās ierīces tirdzniecības iepakojuma attēlu.
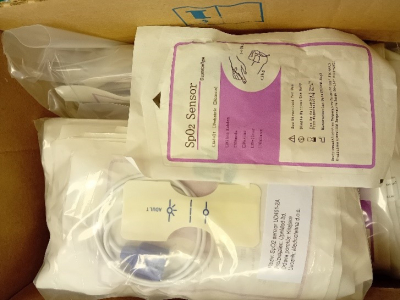
1. fotoattēls ar neatbilstošu etiķeti vienreiz lietojamiem skābekļa piesātinājuma asinīs (SpO2) sensoriem ražotāja
Slovēnijas kompetentā iestāde ir apturējusi vienreiz lietojamo skābekļa piesātinājuma asinīs (SpO2) sensoru laišanu Slovēnijas tirgū, ņemot vērā, sekojošās neatbilstības Regulas 2017/745 prasībām:
Nav CE atbilstības marķējuma;
Etiķetē nav informācijas par ražotāju, ražotāja pilnvaroto pārstāvi Eiropas Savienībā, ražošanas datumu, derīguma termiņu;
Nav ražotāja dokumentācijas (EK atbilstības deklarācija un EK sertifikāts), kas apliecinātu, ka ierīcei ir veikta atbilstības novērtēšanas procedūra atbilstoši Regulas 2017/745 prasībām.

2. fotoattēls. Ražotāja Shenzhen Upnmed Equipment Co Ltd. oriģināla SpO2 sensoru etiķete
Svarīgi:
Inspekcija vērš uzmanību uz Ministru kabineta 2024.gada 15.augusta noteikumu Nr. 461 “Medicīnisko ierīču noteikumi” 9.punktā un 29.punktā noteikto, ka medicīnisko ierīču izplatītāji, kuru komercdarbības vieta reģistrēta Latvijas Republikā, uzsākot darbību, iesniedz Zāļu valsts aģentūrā iesniegumu, kurā norāda šo noteikumu 28.1., 28.2., 28.3. un 28.5. apakšpunktā minēto informāciju, kā arī to medicīnisko ierīču klasifikācijas klasi, ražotāja nosaukumu un juridisko adresi, kuras plānots izplatīt. Gadījumā, ja izplatītājs vai importētājs ir laidis Latvijas tirgū ražotāja Shenzhen Upnmed Equipment Co Ltd. neatbilstošos vienreiz lietojamos skābekļa piesātinājuma asinīs (SpO2) sensorus, aicinām sazināties gan ar piegādātāju, gan ar patērētājiem, lai veiktu preces atgriešanu un izņemšanu no tirgus.
Jautājumu gadījumā aicinām sazināties ar Veselības inspekcijas Medicīnisko ierīču uzraudzības nodaļu pa tālr. 67081611.